一、基本信息
英文名称:K15Q;K15Q self-assembling peptide;
中文名称:K15Q 自组装多肽;磷酸化自组装多肽K15Q;缬氨酰-赖氨酰-缬氨酰-赖氨酰-缬氨酰-赖氨酰-缬氨酰-赖氨酰-磷酸苏氨酰-苏氨酰-赖氨酰-缬氨酰-谷氨酰胺酰-缬氨酰-赖氨酰-缬氨酰-赖氨酰-缬氨酰多肽
氨基酸序列:缬氨酸-赖氨酸-缬氨酸-赖氨酸-缬氨酸-赖氨酸-缬氨酸-赖氨酸-磷酸苏氨酸-苏氨酸-赖氨酸-缬氨酸-谷氨酰胺-缬氨酸-赖氨酸-缬氨酸-赖氨酸-缬氨酸
单字母序列:H₂N-VKVKVKVKVpPTKVQVKVKV-OH
三字母序列:H2N-Val-Lys-Val-Lys-Val-Lys-Val-Lys-Val-DPro-Pro-Thr-Lys-Val-Gln-Val-Lys-Val-Lys-Val-OH
氨基酸长度:18肽
分子量:2230.86 Da
分子式:C106H196N28O23
等电点:pI≈8.9(强碱性,因含多个赖氨酸(Lys)正电荷残基,磷酸化苏氨酸的微弱负电荷、谷氨酰胺(Gln)的中性特征,仅轻微中和部分正电荷,不改变整体强碱性)
结构式:
二、作用机理
K15Q的核心作用依赖其“离子互补+磷酸化苏氨酸修饰调控+Q残基功能调控+两亲性自组装”四重特性,依托磷酸化位点与Q残基的协同功能,具体机理如下:
1. 自组装启动与双重调控:在弱碱性至中性pH值(7.0-8.5)及生理盐离子浓度条件下,K15Q分子间通过Val残基的疏水聚集、Lys⁺与pThr磷酸基团的静电配对、Q残基酰胺基形成的分子间氢键及整体分子间氢键协同作用,启动自组装过程;磷酸化苏氨酸可精准调控分子间静电作用强度,实现自组装速度的可控调节(去磷酸化后组装速度显著加快),Q残基通过形成额外氢键,稳定自组装结构、延缓解组装进程,二者协同实现自组装行为的双重调控;
2. 仿生微环境构建:组装形成的三维水凝胶网络具有高含水量(>90%)、高孔隙率、力学性能稳定的特点,其纳米纤维结构与天然细胞外基质(ECM)高度相似,Q残基的存在可增强水凝胶与细胞外基质蛋白的结合能力,为细胞黏附、铺展、增殖及分化提供稳定支撑,适配神经、软骨、皮肤等多种组织来源细胞的体外培养与体内移植需求;
3. 分子结合与靶向递送功能:K15Q的强碱性(多个Lys⁺)、磷酸化位点(pThr负电)及Q残基的酰胺基,使其可与带负电的生物分子(如DNA、RNA、蛋白、脂质体)发生特异性结合,同时磷酸化苏氨酸可与细胞表面磷酸酶特异性识别,Q残基可与细胞表面含氨基、羧基的受体结合,双重提升靶向递送效率,减少脱靶效应,同时可保护敏感生物分子免受降解;
4. 生物相容性与可降解性:该多肽由天然氨基酸组成,含生理性磷酸化苏氨酸修饰与Q残基,无免疫原性,不会引发机体免疫排斥反应,可被体内蛋白酶(如胰蛋白酶、磷酸酶)逐步降解,磷酸化苏氨酸可被磷酸酶去磷酸化,Q残基可被酰胺酶降解,最终降解为氨基酸、磷酸基团,被机体代谢利用,无残留毒性;
5. 特异性分子识别功能:Q残基的酰胺基可与生物分子(如蛋白、多糖)的功能基团发生特异性氢键结合,使K15Q水凝胶具备一定的分子识别能力,可用于特异性生物分子的包埋与缓释,拓展其在生物传感、靶向递送领域的应用。
三、研究进展
K15Q作为含磷酸化苏氨酸修饰与谷氨酰胺Q特征残基的离子互补型自组装18肽,凭借其双重调控的自组装性能、优异的生物相容性及Q残基的特异性功能,目前已成为生物材料、靶向药物递送、组织工程及分子识别领域的研究热点,核心研究进展集中在三个方向:
一是基础组装特性研究,已明确磷酸化苏氨酸修饰与Q残基对其自组装动力学、构象转变(α-螺旋→β-折叠)及水凝胶力学性能的协同调控规律,证实Q残基可显著提升水凝胶的结构稳定性与分子结合能力,磷酸化修饰可精准调控组装速度,同时明确了溶液浓度、pH值、盐离子强度对其组装性能的影响;
二是应用领域拓展,目前广泛应用于3D细胞培养、核酸/药物靶向递送、组织工程支架(神经、软骨组织再生)、分子识别及生物传感器构建等研究,在神经组织再生领域,K15Q水凝胶的稳定性与神经组织微环境适配,Q残基可增强与神经细胞的黏附,同时可通过磷酸化修饰调控神经细胞分化,提升神经再生效果;在靶向药物递送领域,其磷酸化位点与Q残基的双重靶向作用,可实现药物向病变部位的精准富集,降低全身毒副作用;
三是结构优化与复合应用,目前研究多聚焦于K15Q的磷酸化位点修饰(如双磷酸化修饰)、Q残基修饰,以调节其自组装性能、靶向性及体内半衰期,同时探索其与EAK系列、LK系列、RADA系列多肽及生物活性因子(如神经生长因子、磷酸酶抑制剂)的协同作用,构建“可控组装+靶向递送+分子识别”的复合水凝胶材料,拓展其在临床前研究中的应用场景。整体而言,K15Q因自组装可控、靶向性强、具备分子识别功能,已成为多功能生物材料研究的常用序列,目前仍处于临床前研究阶段,未来重点方向为修饰位点与Q残基的精准调控、规模化制备及临床转化应用,尤其在神经组织再生、特异性靶向治疗等领域具有独特优势与广阔前景。
四、溶解与保存
溶解特性:K15Q为强碱性磷酸化18肽,含疏水性Val残基与Q残基,易溶于超纯水、稀盐酸溶液(0.1%-1%)及PBS缓冲液(pH7.4),溶解时需进行低功率超声辅助溶解(50-100W,5-10分钟),常温缓慢搅拌,避免高温(>30℃)导致多肽变性、磷酸化苏氨酸位点脱落;在高盐浓度(>0.5M NaCl)或强碱性环境(pH>10.0)下,易发生聚集,且可能导致磷酸化位点不稳定,需避免上述极端环境;溶解后需尽快使用,避免长时间放置导致磷酸化位点水解及多肽聚集。
保存条件:粉末状态下,于-20℃干燥避光环境中密封保存,可稳定存放12个月以上,需隔绝空气、湿气与氧化剂,防止磷酸化苏氨酸位点水解、多肽氧化及Q残基变性;水溶液需低温(4℃)短期暂存,存放时间不超过48小时,建议分装保存(每管0.5-1mL),避免反复冻融;长期保存的水溶液需添加适量防腐剂(如0.01%叠氮钠)及磷酸酶抑制剂(如Na₃VO₄),防止微生物污染及磷酸化苏氨酸位点去磷酸化;避免强光照射及高温(>25℃)环境,防止多肽降解、变性、磷酸化位点脱落或自组装结构异常。
五、相关多肽
同属磷酸化自组装多肽及离子互补型多肽体系,且与K15Q序列相似或功能相近的核心相关多肽包括:MAX1(VKVKVKVKVpPTKVEVKVKV,19肽,pThr修饰,含Glu残基、无Q残基)、K15E(序列与K15Q相近,Q残基替换为Glu残基,无Q特征)、KV18(VKVKVKVKVKVKVKVKVKV,18肽,无磷酸化修饰与Q残基,K15Q的未修饰类似物)、EAK16-I(AEAEAKAKAEAEAKAK,16肽,离子互补型,无磷酸化修饰与Q残基)、LK13(LKLKLKLKLKLKL,13肽,强碱性,无磷酸化修饰与Q残基)、pKV-Q(含Q残基的磷酸化KV短肽,10-15肽,K15Q核心序列截短体)。此类多肽中,K15E、KV18与K15Q亲缘性最高,均为KV交替序列,仅在特征残基、磷酸化修饰上存在差异;K15Q相较于MAX1,以Q残基替代Glu残基,分子结合能力与结构稳定性更优,相较于无Q残基的多肽,具备独特的分子识别功能,可根据具体研究需求(如组装调控、靶向递送、分子识别、组织适配性)选择使用。
 网硕互联帮助中心
网硕互联帮助中心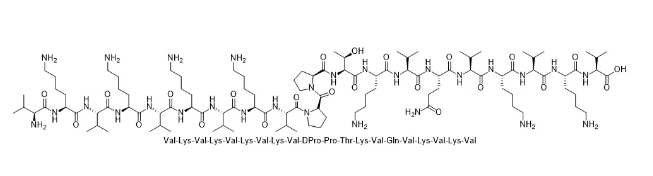




评论前必须登录!
注册